CORROSIE EN ROESTVAST STAAL
Corrosie is meestal een ongewenste aantasting veroorzaakt door agressieve componenten die zich rond of op een metaal bevinden. Alle onedele metalen zijn gevoelig voor corrosie en dat hangt af van het negatieve elektrische potentiaal dat dit metaal heeft. Deze metalen worden ook wel actieve metalen genoemd. De waarden van de elektrische potentialen worden weergegeven in de zogenaamde edelheidreeks (afbeelding 1).
Des te groter de negatieve waarde is, des te heftiger dit metaal reageert met zijn omgeving. Het metaal natrium is dermate onedel, dat het reeds heftig reageert bij blootstelling aan water. Lood (Pb) daarentegen heeft slechts een kleine negatieve potentiaal waardoor het probleemloos twintig jaar meegaat als afdekkingsmetaal op daken.
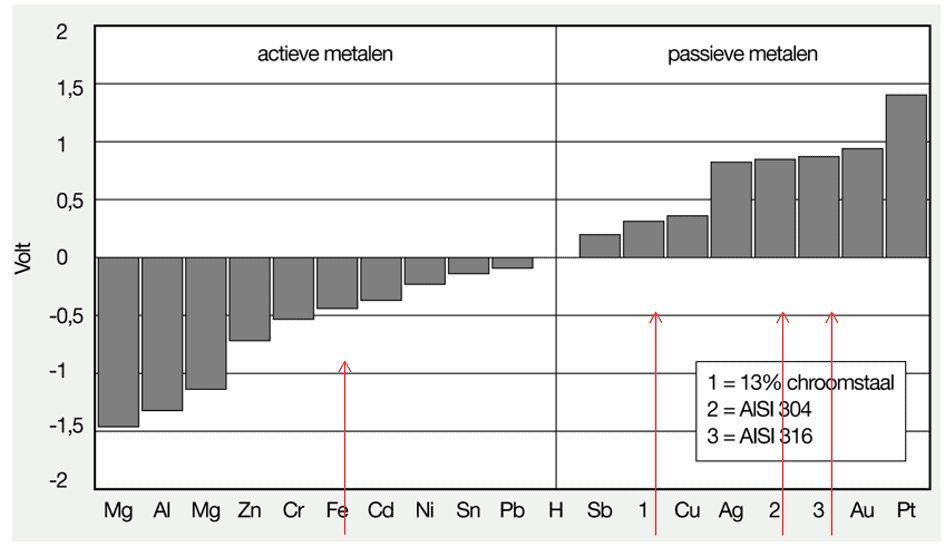
Aluminium (Al) heeft een negatieve elektrische waarde, die circa drie keer groter is dan die van ijzer (Fe). Toch blijkt na verloop van tijd dat een aluminium onderdeel in de buitenlucht best mooi blijft, terwijl ijzer al vrij snel gaat roesten. Met het oog op de potentaalverschillen klinkt dat tegenstrijdig, maar dat is het niet. Aluminium vormt namelijk met zuurstof een dichte oxidehuid die perfect past op het onderliggende metaal. Hierdoor kan het water c.q. elektrolyt niet bij het metaal komen waardoor het mooi blijft. IJzer heeft deze eigenschap niet want de oxidehuid (roest) dat ontstaat, heeft een volume dat wel zeven keer groter is in vergelijking met het onderliggende metaal, waardoor het zich zelf kapot drukt. Daardoor kan het water door deze poreuze laag binnen dringen om een nieuw laagje ijzer aan te tasten. Dit roestproces gaat door totdat al het ijzer geoxideerd is.
Chroom heeft, net als aluminium, ook de eigenschap om een uiterst dun passief oxidelaagje aan het oppervlak te vormen waardoor water niet bij het onderliggende metaal kan komen. Gaat men dit chroom legeren in ijzer, dan zal bij ongeveer 12% chroom ook een beschermend huidje ontstaan. Dit huidje zorgt ervoor dat het staal roestvast wordt. Dit materiaal wordt ook wel chroomstaal genoemd. Het huidje wordt inert omdat het niet meer reageren kan met zijn omgeving. Er is immers chroomoxide ontstaan en dat is feitelijk verbrand chroom. Een lucifer die opgebrand is, kan je niet een tweede keer laten branden en zo is dit ook met chroomoxide. Het metaal is nu passief geworden. Feitelijk kan men beter zeggen dat de huid passief is geworden, maar niet het onderliggende metaal. Daarom moet deze huid goed onderhouden worden teneinde het onderliggende metaal goed te blijven beschermen.
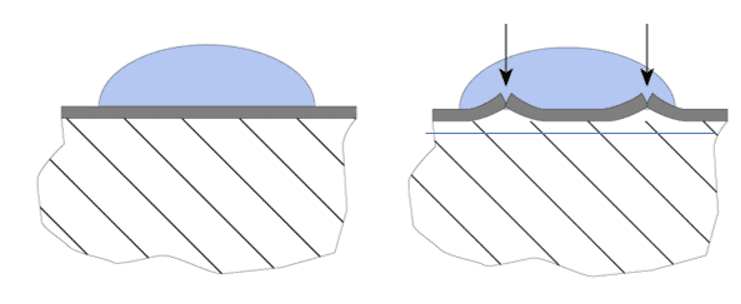
Zo lang deze huid in tact blijft, zal het metaal niet aangetast worden. Zodra het chroomstaal verder wordt gelegeerd met de juiste hoeveelheden nikkel en molybdeen, ontstaan de kwaliteiten AISI304 en 316. Deze legeringen vindt men terug op de plaatsen 1, 2 en 3 in de edelheidsreeks (afbeelding 1. In het begin van deze blog wordt gesteld dat corrosie meestal ongewenst is en dan zou men zich dus kunnen afvragen of er situaties zijn dat corrosie wel gewenst is. Dat is inderdaad het geval als het om opofferingsanodes gaat bij kathodische bescherming. Een goed voorbeeld zijn de zinkanodes die op de buitenwand van een schip worden aangebracht.. Zink (Zn) is onedeler dan staal (Fe) waardoor het zich opoffert ten gunste van het staal (afbeelding 3). Zo wordt de scheepshuid beschermd dankzij galvanische corrosie die in dit geval dus gewenst is.
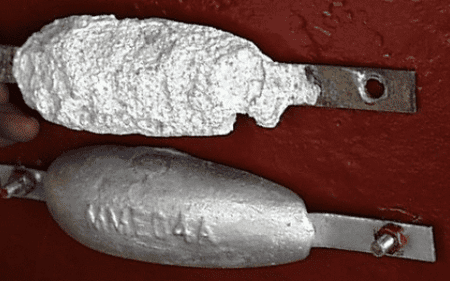
Corrosie van roestvast staal.
Er zijn diverse vormen van corrosie en onderstaand worden een aantal typen opgesomd. Veel genoemde typen zijn van toepassing bij een ondoordacht gebruik van roestvast staal. Hierbij kan gedacht worden aan:
- Algemene corrosie
- Interkristallijne corrosie
- Knife-line attack
- Spanningscorrosie ofwel transkristallijne corrosie
- Putvormige corrosie
- Spleetcorrosie
- Lasbederf ofwel ‘weld decay’
- Besmettingscorrosie ofwel contaminatie
- Microbieel geïnduceerde corrosie
- Galvanische corrosie
- Hoge temperatuur corrosie
Daarom is de term ‘roestvrij staal’ niet juist; de naam ‘roestvast staal’ is een veel betere keuze. Roestvast wil zeggen dat het metaal een bepaalde vastheid geniet tegen corrosie mits aan de voorwaarden wordt voldaan. Dan kan dit metaal wel een mensenleven meegaan. Respecteert men die voorwaarden niet of onvoldoende, dan kan het al naar enige weken of maanden gaan corroderen.
Heeft u nog vragen over het toepassen van bepaalde RVS kwaliteiten of andere legeringen?
Metaalselector is een computerprogramma dat in eigen beheer ontwikkeld is om een juiste keuze te maken op basis van corrosie- en materiaal eigenschappen.
Ga naar Metaalselector.nl voor meer informatie en om eigen toegang te krijgen tot dit programma, waarmee u een eigen gedegen materiaalkeuze kunt maken voor uw toepassingen.
Vind hier ook mijn blogs welke geschreven zijn voor AluRVS: https://www.alurvs.nl/roestvast-staal/Blog/
en AluRVS Staal: https://www.alurvs.nl/staal/blog/
