HET BEREIDEN VAN STAAL
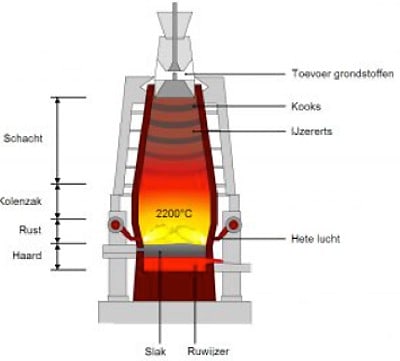
In een hoogoven wordt van ijzererts, ruw ijzer gemaakt. Op een vereenvoudigende korte wijze wordt onderstaand een overzicht gegeven hoe ijzererts wordt omgezet naar ruw ijzer. IJzererts bestaat voor een groot deel uit ijzeroxide en dat wordt als een bruinachtige aarde gedolven in ijzermijnen. Ook bevat het ijzererts verontreinigingen en daarom wordt er in de hoogoven een bepaalde toeslag gechargeerd om deze stoffen te binden. Het ijzererts wordt vermengd met cokes dat een dubbele functie heeft.
Cokes dient als brandstof om het geheel in de hoogoven te verhitten en tevens is het een reductiemiddel om het ijzeroxide om te zetten in ruw ijzer. Dit gebeurt volgens de chemische formule 2FeO + C + e → 2Fe +CO2. Dit is tevens de reden dat een hoogoven veel gasvormig koolzuur (CO2) uitstoot. Deze uitstoot levert steeds meer maatschappelijke onrust en weerstand op. Daarom wordt er tegenwoordig ook geëxperimenteerd met waterstof als reductiemiddel. Dan verloopt de reactie als volgt: FeO + H2 + e → Fe +H2O. Milieutechnisch is dat een prachtige oplossing maar deze ontwikkeling staat nog voor een deel in de kinderschoenen. Beide scheikundige reacties zijn endotherm van aard. Cokes worden gemaakt door vergruisd steenkool te verhitten tot circa 1000°C zonder dat er zuurstof bij kan komen. Hierdoor ontstaat een kraakproces, die vluchtige stoffen opleveren en cokes.
Het ruwe ijzer gaat in gesmolten toestand in een peervormig vat naar de oxystaalfabriek waar door raffinage uiteindelijk koolstofstaal wordt gemaakt. Ruw ijzer bevat ongeveer 4% koolstof, waardoor dit materiaal veel te bros is om het te kunnen gebruiken. In de oxystaalfabriek staat een convertor waarin dit gesmolten ruwe ijzer wordt geladen samen met ongeveer 25% staalschroot. Men blaast dan met een watergekoelde lans pure zuurstof in het smeltbad waardoor het koolstof voor een groot deel verbrandt wordt tot koolzuur (CO2). Hierbij komt zoveel warmte vrij dat de convertor zichzelf op de gewenste temperatuur kan houden. Het kan zelfs te heet worden en dan wordt er meer koud staalschroot gechargeerd want dat doet de absolute temperatuur van de smelt weer dalen. Naast koolstof worden ook andere elementen verbrandt zoals stikstof, zwavel en fosfor. Zodra deze stoffen verbrand zijn, komen deze in de slaklaag terecht die bovenop de smelt drijft.
Uiteraard houdt de smeltmeester in de gaten dat het koolstofgehalte niet te laag wordt. Na afloop gaat het gesmolten metaal in een staalpan. Er wordt argongas vanuit de bodem in de smelt geblazen waardoor dit gas een soort roerfunctie krijgt. Het gevolg van al die gebruikte gassen is, dat er veel gasbelletjes in het gesmolten metaal aanwezig zijn. Als dit zo blijft, dan zal het staal ongewenst poreus worden. Er wordt dan gesteld dat het staal onrustig is, dus moeten er maatregelen genomen worden. Dat kan met een vacuümtechniek maar ook door toevoeging van enig aluminium of ferrosilicium dat door het aanwezige zuurstof wordt geoxideerd. Omdat het staal op deze wijze de gasbelletjes kwijtraakt, komt de smelt tot rust. Dit wordt gekalmeerd staal genoemd. Gekalmeerd staal heeft een homogene samenstelling gekregen en daardoor ook gelijkmatige mechanische eigenschappen. Zo ontstaat koolstofstaal dat taai en ductiel is zodat het goed smeedbaar, bewerkbaar en lasbaar is. Tenslotte kunnen ook legeringselementen zoals chroom, nikkel en mangaan aan het staal worden toegevoegd. Dat hangt er uiteraard vanaf welke legering gewenst is. Nadat er dikke plakken en billets van gemaakt zijn, kan men het staal verder verwerken tot de gewenste producten. Veelal gaat dit verwerken om het wals- en extrusieproces.
Terug naar de natuurlijke situatie
Natuurwetten leren ons dat energie niet verloren gaat en dat ieder systeem streeft naar de laagste energetische toestand. Uit de scheikundige formules blijkt, dat er energie nodig is om de reductie van ijzeroxide mogelijk te maken. M.a.w. het bereidde ijzer wil weer heel graag terug naar zijn stabiele natuurlijke situatie en dat is dus ijzeroxide. Dit kan droog plaatsvinden, wat vooral bij hoge temperatuur gebeurd volgens de formule Fe + O2 → 2FeO + energie of door een nat-chemisch proces volgens de scheikundige reactie 2Fe + 2H2O + O2 → 2Fe(OH)2 + energie. Dat betekent dat de energie die door de hoogoven geleverd is, weer wordt teruggegeven aan de hand van deze exothermische reacties. Het materiaal oxideert en daarbij komt warmte vrij. Uiteraard wil men dit oxidatieproces voorkomen en dat kan door het staal van een beschermende coating te voorzien. Ook kan het bijvoorbeeld verzinkt of geplastificeerd worden.
Het veredelen van staal
Het veredelen van staal begint met een hardingsproces. Dat betekent dat het materiaal qua temperatuur zich in het austenietgebied bevindt. Bij die hoge temperatuur wordt het staal afgeschrikt in een koelmiddel, waarna het ontlaten wordt bij een temperatuur van circa 450°C. Op deze wijze wordt een gunstige combinatie van taaiheid en trekvastheid verkregen. Het materiaal is dan veredeld. De mechanische eigenschappen worden verhoogd alsmede ook de elasticiteit.
Zilverstaal
Zilverstaal heeft niets met zilver te maken, maar het is op hoogglans geslepen stafmateriaal van gelegeerd koolstofstaal met een diameter van circa 1 tot 30 mm. Het wordt gebruikt voor de vervaardiging van speciale boren, asjes en kleine onderdelen in de instrumenten- en apparatenbouw. Het is meestal in twee kwaliteiten leverbaar t.w. ongelegeerd met circa 1% koolstof zoals EN 1.1545 en gelegeerd zilverstaal zoals EN 1.2510 en 1.2842.
Vind hier ook mijn blogs welke geschreven zijn voor AluRVS Staal: https://www.alurvs.nl/staal/blog/

[…] Deze verbindingen hebben een eigen kristalrooster en zijn in de regel hard en bros. Hun aanwezigheid vergroot de mechanische sterkte, maar het gaat wel ten koste van de vervormbaarheid van de ontstane tweefasige legering. Wanneer omvormen belangrijk is, moet het totale percentage legeringselementen daarom voldoende laag gehouden worden, bijvoorbeeld niet meer dan zo'n 3 tot maximaal 8%. De meeste in de techniek toegepaste aluminiumlegeringen, zijn op zich best gecompliceerd qua samenstelling. Gewoonlijk bevatten deze een of twee hoofdlegeringselementen, die vooral het niveau van de mechanische eigenschappen bepalen. Daarnaast komen er dan nog een aantal secundaire legeringselementen voor in kleinere hoeveelheden. Die kunnen zijn toegevoegd om bepaalde eigenschappen te bereiken. Een voorbeeld hiervan is een fijnere korrelgrootte die ontstaat door de toevoeging van natrium aan aluminiumsiliciumlegeringen. Bepaalde elementen kunnen echter ook als verontreiniging in het metaal achtergebleven zijn, zoals bijvoorbeeld ijzer na elektrolyse van nieuw aluminium en koper na het omsmelten van schroot. Door toevoeging van 0,1 tot 0,3% chroom aan het aluminium, wordt het ijzer dat bij de elektrolyse is achtergebleven, in een minder schadelijke vorm afgescheiden. Omdat mangaan hetzelfde effect geeft, wordt chroom vaak samen met mangaan toegevoegd. Voorts vermindert chroom de gevoeligheid voor spanningscorrosie van aluminium/zink/magnesiumlegeringen omdat de precipitatie op de korrelgrenzen en in de korrels er homogener van worden. Net als chroom, vermindert koper de gevoeligheid voor spanningscorrosie van aluminium/zink/magnesiumlegeringen. Indien de mechanische bewerkbaarheid verbeterd moet worden dan kan dat bereikt worden door enig lood te legeren. Aluminium wordt ook gebruikt bij het bereiden van staal. Het wordt vooral gebruikt bij de hoogovens om het staal te kalmeren. Zie het blog "het bereiden van Staal" […]