HET CHLORIDEGEHALTE VERSUS ROESTVAST STAAL
Chloor is een element dat behoort tot de groep halogenen en dat zijn per definitie zoutvormers. Andere bekende elementen die tot deze groep behoren zijn fluor, broom en jodium. Halogenen bezitten een grote reactiviteit waardoor deze elementen niet vrij in de natuur voorkomen maar altijd als een verbinding. Fluorverbindingen komen het meest voor in de natuur.
Alle elementen, die tot de halogenen worden gerekend, hebben chemisch gezien veel gemeenschappelijk. Een voorbeeld hiervan is dat alle halogenen zeven electronen bezitten in de buitenste schil van het atoom. Hierdoor kunnen ze zeer gemakkelijk een elektron opnemen van een ander element. Door dit ontvangende vermogen van een vreemd elektron zijn halogenen per definitie reactieve stoffen. Fluor en chloor zijn de meest reactieve halogenen. Met metalen maken ze gemakkelijk een verbinding en in het bijzonder met alkalimetalen. Het gevolg is dan het aantasten van het betreffende metaal. Alkali-metalen zijn overigens de meest onedele metalen die er bestaan. Enige voorbeelden hiervan zijn natrium, kalium, cesium en lithium.
Deze elementen reageren het heftigst met halogenen. Ook andere onedele metalen kunnen aangetast worden door halogenen maar niet zo heftig als de metalen uit de alkaligroep. Dit aantasten wordt vooral veroorzaakt door het element chloor. Het ion van chloor is het chloride-ion, dat kortweg chloride wordt genoemd. Edele metalen worden in principe niet aangetast door halogenen.Zoals hierboven reeds is gesteld, kunnen naast alkalimetalen ook andere onedele metalen worden aangetast. In deze blog beperken we ons tot roestvast staal. Het klinkt wellicht wat vreemd om roestvast staal te rekenen tot de onedele metalen maar toch is dat op zich terecht. De grondmassa heeft in de edelheidsreeks een negatieve potentiaal en dan wordt zo’n matrix onder de onedele metalen geschaard. Dit geldt echter niet voor de dunne chroomoxidehuid die zich rondom het roestvast staal bevindt. Deze oxidehuid is wel passief c.q. edel waardoor de potentiaal zich wel in het edele gebied bevindt. Daarom gedraagt roestvast staal zich edel en mag het zich nestelen tussen de edele metalen dankzij deze voortreffelijke oxidehuid. Het materiaal is nu corrosiebestendig geworden. De voorwaarde is wel dat de chloridebelasting niet te hoog mag oplopen.
Valt deze binnen acceptabele grenzen, dan weerstaat deze oxidehuid probleemloos een nat chemisch milieu dat chloriden bevat. Wordt het chloridegehalte te hoog, dan zullen de zwakste plekken in de oxidehuid bezwijken waardoor er op die plek corrosie ontstaat. Dat wordt dan putcorrosie of ook wel pitting genoemd. Daarbij speelt ook de temperatuur een grote rol want zodra deze gaat stijgen, neemt de reactiviteit sterk toe in een soort parabolische functie. Tenslotte heeft de chemische samenstelling van het roestvast staal een grote invloed op de corrosieprestaties. Het element molybdeen zorgt er namelijk voor dat de weerstand tegen chloriden aanzienlijk toeneemt.
Op onderstaande grafiek is indicatief aangegeven tot hoeverre een bepaalde familie roestvast staal corrosief belast mag worden in afhankelijkheid van de temperatuur en het chloridegehalte. De rode lijn geeft de begrenzing aan voor de AISI304 kwaliteiten terwijl de blauwe lijn dit aangeeft voor de AISI316 familie. De groene lijn geeft de begrenzing aan voor het hoogwaardige 904L (EN 1.4539). Boven die grens zal men aan nog hoogwaardiger metalen moeten denken zoals superduplex, titanium en nikkellegeringen. Veronderstel dat men een watertype heeft met 200 ppm (mg/liter) chloride. Dat betekent dat roestvast staal AISI 304 niet warmer mag worden dan 40°C. Zodra AISI316 wordt toegepast, beschikt de legering over 2% molybdeen waardoor deze temperatuur verhoogd mag worden tot 70°C. Bij een chloridegehalte van 1000 ppm (1000 mg/liter) mag AISI304 niet warmer worden belast dan 10°C en AISI316 tot iets boven de 20°C. Uit de grafiek blijkt ook dat het super austenitische materiaal 904L tot 80°C blootgesteld mag worden aan dit corrosieve milieu. Hieruit blijkt hoe superieur deze hoogwaardige kwaliteit roestvast staal is t.o.v. de gebruikelijke typen. RVS 904L bevat 23-28% nikkel, 19-23% chroom, 4-5% molybdeen en 1-2% koper.
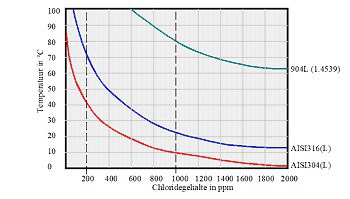
Men moet altijd rekening houden dat corrosiediagrammen ook met de nodige voorzichtigheid gebruikt moeten worden. De resultaten geven slechts een indicatie aan met ideale omstandigheden. In de praktijk kunnen nog wel eens door onvoorzienbare omstandigheden andere factoren een rol spelen die niet in dergelijke diagrammen te vangen zijn. Hierbij kan gedacht worden aan wel of geen beluchting en grote schommelingen van temperaturen. Ook mogelijke chemische stoffen die in geringe mate extra aanwezig kunnen zijn, zullen de corrosie kunnen versnellen maar ook vertragen. Bij dit laatste wordt gedacht aan stoffen die het bufferend vermogen van het water beïnvloeden waardoor er een inhibiterende c.q. corrosieremmende werking van uit kan gaan.
Heeft u nog vragen over het toepassen van bepaalde RVS kwaliteiten of andere legeringen?
Metaalselector is een computerprogramma dat in eigen beheer ontwikkeld is om een juiste keuze te maken op basis van corrosie- en materiaal eigenschappen.
Ga naar Metaalselector.nl voor meer informatie en om eigen toegang te krijgen tot dit programma, waarmee u een eigen gedegen materiaalkeuze kunt maken voor uw toepassingen.
Vind hier ook mijn blogs welke geschreven zijn voor AluRVS: https://www.alurvs.nl/roestvast-staal/Blog/
en AluRVS Staal: https://www.alurvs.nl/staal/blog/

[…] de blog “het chloridegehalte versus roestvast staal” zijn we vooral ingegaan over de toepasbaarheid van roestvast staal in milieus die chloriden […]